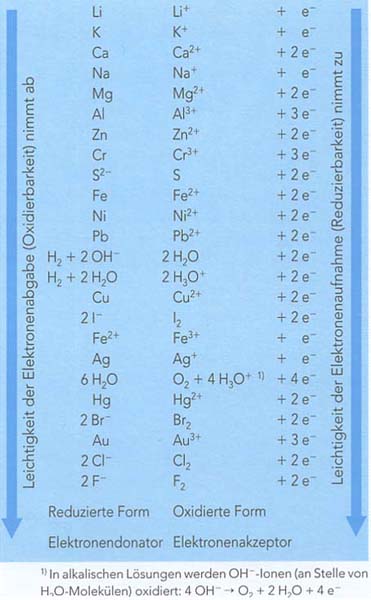
Redoxreihe der Metalle
Wie edel oder unedel ein Metall ist, hängt von seiner Tendenz, in Redoxreaktionen Elektronen abzugeben, ab.
Je nach Reaktionspartner kann ein Metall-Ion sowohl ein Reduktionsmittel sein, das oxidiert wird, als auch ein Oxidationsmittel, das reduziert wird. (Donator-Akzeptor-Reaktionen)
Das System aus Reduktor und dem zugehörigen Oxidator wird als korrespondierendes Redoxpaar bezeichnet.
Ordnet man nun alle korrespondierenden Redoxpaare entweder nach dem Reduktionsvermögen der Metall-Atome oder dem Oxidationsvermögen der Metall-Ionen, erhält man diese Reihenfolge:
Anmerkung: Diese Tabelle listet sowohl Metalle als auch Nichtmetalle auf !
Am oberen Ende der Redoxreihe sind Metalle zu finden, welche die stärksten Elektronen-Donatoren sind.
Analog dazu finden sich am unteren Ende der Reihe die Edelmetalle, welche die stärksten Elektronen-Akzeptoren sind.
Das Redoxpaar Wasserstoff/Oxonium-Ionen nimmt eine besondere Stellung innerhalb der Redoxreihe ein.
Es bildet die Trennlinie zwischen den sogenannten "unedlen" bzw "edlen" Metallen.
Metalle, deren Atome von Oxonium-Ionen oxidiert werden, bezeichnet man als unedel; Metalle, die nicht von Oxonium-Ionen oxidiert werden, bezeichnet man als edel.
Siehe auch:
Literaturverzeichnis
[1] Tausch, Michael: Chemie SII. Stoff - Formel - Umwelt, Aus: C.C.Buchner, Bamberg 2008, S. 169-171