Quantitative Redoxreihe
Bei der Kombination zweier beliebiger Redoxpaare kann immer eine spezifische Spannung gemessen werden, die sogenannte Potentialdifferenz.
Dabei gilt: Je weiter die Redoxpaare in der Redoxreihe auseinanderstehen, desto größer ist die Spannung zwischen den betreffenden Halbzellen.
Außerdem lassen sich entsprechende Spannungen addieren, d.h. die Spannung einer Zink-Silber-Zelle entspricht den Spannungen für die Zink-Blei und die Blei-Silber-Zelle
Jedem Redoxpaar kann ein spezifischer Potential-Wert in Bezug auf ein bestimmtes Redoxpaar zugeordnet werden.
Diesen Bezugspunkt stellt die Standard-Wasserstoff-Halbzelle dar.
Die unter Standard-Bedingungen gemessene Potentialdifferenz zwischen einer beliebigen Halbzelle und der Standard-Wasserstoff-Halbzelle bezeichnet man als Standard-Elektroden-Potential oder Normalpotential.
Redoxpaare, die gegenüber der Standard-Wasserstoff-Halbzelle den elektrisch negativen Pol bilden, erhalten einen negativen Potentialwert, wobei Redoxpaaren, die gegenüber der Standard-Wasserstoff-Halbzelle den elektrisch positiven Pol bilden, ein positiver Potentialwert zugeordnet wird.
Daraus ergibt sich die Spannungsreihe der Metalle: Bild gelöscht!
Anhand der Standard-Elektronen-Potentiale können wir nun die Zellspannung jeder beliebigen galvanischen Zelle (Galvanische Zelle) unter Standardbedingungen bestimmen.
Die Zellspannung U ergibt sich aus der Differenz der Standard-Elektroden-Potentiale:
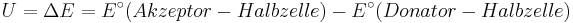
Das Standard-Elektroden-Potential ist also ein quantitatives Maß für die Neigung der Metall-Atome, als Elektronen-Donatoren zu wirken.
Literaturverzeichnis
[1] Tausch, Michael: Chemie SII. Stoff - Formel - Umwelt, Aus: C.C.Buchner, Bamberg 2008, S. 176-178

