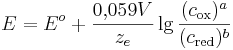Nernst-Gleichung: Unterschied zwischen den Versionen
Aus KAS-Wiki
| Zeile 3: | Zeile 3: | ||
<br /> | <br /> | ||
<math>E = E^\circ + \frac{RT}{z_e F}\ln\frac{a_\mathrm{Ox}}{a_\mathrm{Red}}</math> <br /> | <math>E = E^\circ + \frac{RT}{z_e F}\ln\frac{a_\mathrm{Ox}}{a_\mathrm{Red}}</math> <br /> | ||
| + | <br /> | ||
| + | Unter Standardbedingungen vereinfacht sich die Nernst-Gleichung und man betrachtet nur noch die Abhängigkeit von der Konzentration. <br /> | ||
| + | <br /> | ||
| + | <math>E = E^{o}+\frac{0{,}059 V}{z_e}\lg\frac{(c_\mathrm{ox})^a}{(c_\mathrm{red})^b}</math> <br /> | ||
Version vom 14. Dezember 2009, 10:27 Uhr
Die Nernst-Gleichung beschreibt den Einfluss der Konzentration auf das Potential eines Redoxsystems.
Allgemein lässt sich die Nernst-Gleichung wie folgt formulieren:
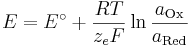
Unter Standardbedingungen vereinfacht sich die Nernst-Gleichung und man betrachtet nur noch die Abhängigkeit von der Konzentration.