Elektrolyse und Faraday-Gesetze
Elektrolyse
Als Elektrolyse wird eine durch elektrischen Strom erzwungene Redoxreaktion bezeichnet. Hierbei laufen Oxidation und Reduktion räumlich von einander getrennt ab. Am Besten wird dies an einem Beispiel deutlich:
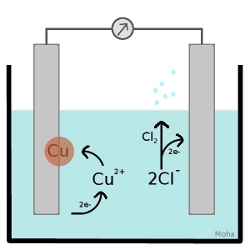
In ein Becherglas wird eine Kupfer-(II)-Chlorid-Lösung gegeben und zwei Metallstäbe werden in die Lösung gestellt, welche die Elektroden darstellen. Diese sind mit Kabeln an eine Spannungsquelle angeschlossen. Um welche Metalle es sich hierbei handelt ist nicht von Wichtigkeit.
Aufgrund der Redoxreihe der Metalle werden die Kupferionen zum Elektronenakzeptor und die Chloridionen zum Elektronendonator, d.h. die Kupferionen werden zu elementarem Kupfer reduziert. Dieser Vorgang findet an der Kathode statt, die bei der Elektrolyse negativ geladen ist. Im Gegensatz dazu werden die Chloridionen an der Anode oxidiert und ein geschlossener Stromkreis entsteht, der elementares Kupfer und molekulares Chlor entstehen lässt.
Kathode: Cu2+(aq) + 2e- ------> Cu(s)
Anode: 2Cl-(aq) ------> Cl2(g) + 2e-
Gesamt: Cu2+(aq) + 2Cl-(aq) ------> Cu(s)+ Cl2(g)
Faraday-Gesetze
Michael Faraday hat durch seine Forschungen einen großen Teil zu den heute bekannten Gesetzmäßigkeiten beim Ablauf einer Elektrolyse beigetragen und zwei nach ihm benannte Gesetze aufgestellt:
1. Faraday-Gesetz:
Die elektrolytisch abgeschiedenen Stoffmengen sind der durch den Stromkreis geflossenen Ladung Proportional.[1]
2. Faraday-Gesetz:
Zur elektrolytischen Abscheidung einer bestimmten Stoffmenge n eines Stoffes wird die Ladung Q=n*z*F benötigt, wobei z die Anzahl der an der Elektrode pro Ion übertragenen Elektronen bedeutet. (F=96487 C*mol-1)[2]